América Latina /
Áreas de Produtos /
Acesso vascular /
Acesso central /
Cateteres Venosos Centrais (CVC) curta permanência

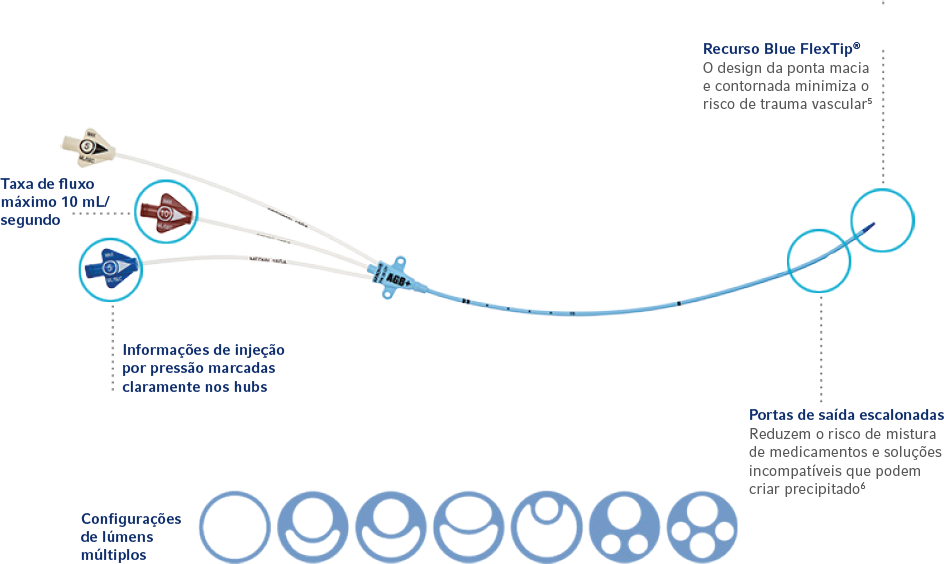
CVC Arrowg+ard Blue Plus®
Ajude a proteger seus pacientes de complicações relacionadas a cateteres.
O CVC Arrowg+ard Blue Plus® é o único CVC antimicrobiano de espectro completo que protege contra:
- Bactérias Gram-positivas
- Bactérias Gram-negativas
- Fungos
A proteção do Arrowg+ard Blue Plus® está quimicamente ligada ao cateter, fornecendo proteção antimicrobiana na superfície do cateter.
- Cobertura completa – linhas de extensão, hub e cateter protegidos1
- Desempenho in vitro – eficácia comprovada contra "super bugs" comuns resistentes a antibióticos “super bugs”2
Atende às diretrizes e recomendações:
- Centros de Controle de Doenças (CDC)*3
- The Society for Healthcare Epidemiology of America (SHEA)**4

Referências:
- https://www.accessdata.fda.gov/cdrh_docs/pdf/K993691.pdf
- Gupta N, Weber H, Moss S, Gaire-Patel K. Are antibiotic resistant “super bugs” a real challenge to antimicrobial central venous catheter performance? AVA 2014.
- O’Grady NP, Alexander M, Burns LA, Dellinger P, Garland J, Heard SO et al Guidelines for the Prevention of Intravascular Catheter-related Infections, 2011. The Centers for Disease Control. www.cdc.gov/hicpac/pdf/guidelines/bsi-guidelines-2011.pdf
- Buetti, N., Marschall, J., Drees, M., Fakih, M., Hadaway, L., Maragakis, L., . . . Mermel, L. (2022). Strategies to prevent central line-associated bloodstream infections in acute-care hospitals: 2022 Update. Infection Control & Hospital Epidemiology, 1-17. doi:10.1017/ice.2022.87
- Rosenbauer KA, Herzer JA. Surface morphology and tensile force at breaking point or different kinds of intravenous catheters before and after usage. Scan Electron Microsc. 1981;(Pt 3):125-30.
- Collins JL, Lutz RJ. In vitro Study of Simultaneous Infusion of Incompatible Drugs in Multilumen Catheters. Heart & Lung. 1991; 20(3):271-7.
*Use um CVC impregnado com clorexidina/sulfadiazina de prata ou
minociclina/rifampicina em pacientes cujo cateter deve
permanecer no local >5 dias se, após a implementação bem-sucedida de uma estratégia abrangente
para reduzir as taxas de
CLABSI, a taxa de CLABSI não estiver diminuindo.
**Use esses cateteres nas seguintes situações: i. Unidades hospitalares ou populações de pacientes que apresentam uma taxa de CLABSI acima das metas institucionais, apesar da conformidade com as práticas básicas de prevenção de CLABSI. Algumas evidências sugerem que o uso de CVCs antimicrobianos pode não ter nenhum benefício adicional em unidades de atendimento ao paciente que já estabeleceram uma baixa incidência de infecções por cateter. ii. Os pacientes têm acesso venoso limitado e uma história de CLABSI recorrente. iii. Os pacientes apresentam risco aumentado de sequelas graves de um CLABSI (por ex., pacientes com dispositivos intravasculares implantados recentemente, como uma válvula cardíaca protética ou enxerto aórtico)
Contraindicação:
O CVC Arrowg+ard Blue Plus® é contraindicado em pacientes com hipersensibilidade conhecida a medicamentos contendo clorexidina e sulfadiazina de prata e/ou sulfa.
A Lei Federal (EUA) restringe a venda desse produto por pedido de um médico.
Teleflex, o logotipo da Teleflex e Arrow, Arrowg+ard Blue Plus e Blue FlexTip são marcas comerciais ou marcas registradas da Teleflex Incorporated ou de suas afiliadas, nos EUA e/ou em outros países. Todas as outras marcas comerciais são marcas de seus respectivos proprietários. Consulte o status da aprovação regulatória local. Consulte as Instruções de Uso aplicáveis para obter as indicações aprovadas na sua região.
As informações contidas neste documento não são um substituto para as Instruções de uso do produto. Este documento não significa compatibilidade entre dispositivos. É possível que nem todos os produtos estejam disponíveis em todos os países. Entre em contato com seu representante local. Revisado: 08/2022. ©2022 Teleflex Incorporated. Todos os direitos reservados. MC-007978 LA EN
**Use esses cateteres nas seguintes situações: i. Unidades hospitalares ou populações de pacientes que apresentam uma taxa de CLABSI acima das metas institucionais, apesar da conformidade com as práticas básicas de prevenção de CLABSI. Algumas evidências sugerem que o uso de CVCs antimicrobianos pode não ter nenhum benefício adicional em unidades de atendimento ao paciente que já estabeleceram uma baixa incidência de infecções por cateter. ii. Os pacientes têm acesso venoso limitado e uma história de CLABSI recorrente. iii. Os pacientes apresentam risco aumentado de sequelas graves de um CLABSI (por ex., pacientes com dispositivos intravasculares implantados recentemente, como uma válvula cardíaca protética ou enxerto aórtico)
Contraindicação:
O CVC Arrowg+ard Blue Plus® é contraindicado em pacientes com hipersensibilidade conhecida a medicamentos contendo clorexidina e sulfadiazina de prata e/ou sulfa.
A Lei Federal (EUA) restringe a venda desse produto por pedido de um médico.
Teleflex, o logotipo da Teleflex e Arrow, Arrowg+ard Blue Plus e Blue FlexTip são marcas comerciais ou marcas registradas da Teleflex Incorporated ou de suas afiliadas, nos EUA e/ou em outros países. Todas as outras marcas comerciais são marcas de seus respectivos proprietários. Consulte o status da aprovação regulatória local. Consulte as Instruções de Uso aplicáveis para obter as indicações aprovadas na sua região.
As informações contidas neste documento não são um substituto para as Instruções de uso do produto. Este documento não significa compatibilidade entre dispositivos. É possível que nem todos os produtos estejam disponíveis em todos os países. Entre em contato com seu representante local. Revisado: 08/2022. ©2022 Teleflex Incorporated. Todos os direitos reservados. MC-007978 LA EN