
MANTA® Dispositivo de cierre vascular
El Dispositivo MANTA® es el primer dispositivo de cierre vascular biomecánico disponible comercialmente diseñado específicamente para el cierre de sitios de acceso por la arteria femoral de gran diámetro.1 Disponible en 14 Fr. y 18 Fr., un único dispositivo MANTA® cierra eficazmente los sitios de acceso por la arteria femoral luego del uso de vainas que van desde 12 Fr. a 25 Fr. de diámetro exterior.2a
Despliegue simple
Aborda los desafíos del cierre de gran diámetro con un dispositivo simple de usar.2a
Hemostasia rápida
Reduce el tiempo para lograr la hemostasia sin cierre previo, mediante el uso de las propiedades
inductoras de la coagulación del colágeno para una hemostasia rápida con el fin de acelerar la
cicatrización del vaso.2c,3-5
Cierre confiable
Produce resultados reproducibles y ayuda a inspirar confianza en el logro de un cierre
confiable.2b

Clínicamente probado
El Ensayo Clínico SAFE MANTA IDE, el estudio multicéntrico prospectivo más grande de los EE. UU. sobre un dispositivo de cierre de sitios de acceso arterial femoral de gran diámetro diseñado con un propósito hasta la fecha, demostró la seguridad y eficacia del dispositivo MANTA® con el cumplimiento de todos los criterios de valoración primarios y secundarios.2

Características del producto
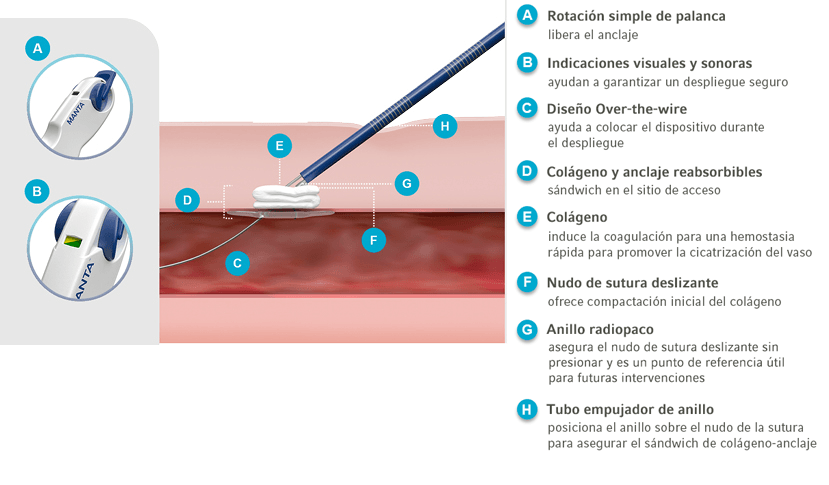
Características y beneficios de MANTA®
Conozca más sobre el dispositivo MANTA®
References:
- Data on file at Teleflex.
- Data on file at Teleflex. The SAFE MANTA IDE Clinical Trial.
a. A single MANTA™ Vascular Closure Device was deployed in 99.6% of subjects in IDE trial.
b. 97.7% Technical Success, defined as percutaneous vascular closure obtained with the MANTA™ Device without the use of unplanned endovascular or surgical intervention.
c. The MANTA™ Device demonstrated a time to hemostasis (TTH) of 24 seconds median time (65 seconds mean time) from deployment to hemostasis, which is lower than published rates for Perclose ProGlide® where Perclose ProGlide® demonstrated a TTH of 9.8 +/- 17 minutes (588 +/- 1,020 seconds).3
d. Major Complications defined as composite of: i) vascular injury requiring surgical repair/stent-graft; ii) bleeding requiring transfusion; iii) lower extremity ischemia requiring surgical repair/additional percutaneous intervention; iv) nerve injury (permanent or requiring surgical repair); and v) infection requiring IV antibiotics and/or extended hospitalization.
Study sponsored by Teleflex Incorporated or its affiliates. - Nelson PR, et al. A multicenter, randomized, controlled trial of totally percutaneous access versus open femoral exposure for endovascular aortic aneurysm repair (the PEVAR trial). J Vasc Surg. 2014 May;59(5):1081-1193.
- Farndale RW, Sixma JJ, Barnes MJ, de Groot, PG. The role of collagen in thrombosis and hemostasis, J Thromb Haemost. 2004 Apr,2(4);564-573.
- Nuyttens BP, Thijs T, Deckmyn H, Broos K. Platelet adhesion to collagen, Thromb Res. 2011;127(2); S26-S29.
- Généreux P, et al. Vascular complications after transcatheter aortic valve replacement. J Am Coll Cardiol. 2012 Sept 18;60(12):1043-1052.
- Lauten A, et al. Percutaneous left-ventricular support with the Impella 2.5-assist device in acute cardiogenic shock: results of the Impella-EUROSHOCK-registry. Circ Heart Fail. 2013 Jan;6(1):23-30.
CONTRAINDICACIONES: No se conocen contraindicaciones para el uso de este dispositivo.
ADVERTENCIAS: 1) No se debe utilizar si el sitio de punción es próximo al ligamento inguinal o está por encima del borde más inferior de la arteria epigástrica (IEA), ya que esto puede provocar sangrado retroperitoneal. 2) No utilizar en pacientes con calcificación grave del vaso de acceso y/o estenosis común de la arteria femoral, lo que resulta en un vaso <5 mm de diámetro para 14F MANTA o <6 mm de diámetro para 18F MANTA, o>50 % de diámetro de la arteria femoral o ilíaca. 3) No utilizar en pacientes con enfermedad vascular periférica grave, como lo demuestra una claudicación grave cuando se caminan <100 pies, pulsos débiles o ausentes en la extremidad afectada, o ABI <0.5 en reposo. 4) No lo utilice si el punto del indicador de temperatura del paquete ha cambiado de gris claro a gris oscuro o negro. 5) No lo utilice si el paquete está dañado o alguna parte del paquete se ha abierto previamente. 6) No utilice si los artículos del paquete parecen dañados o defectuosos de alguna manera. 7) No REUTILICE ni REESTERILICE. El dispositivo MANTA es de un solo uso. El dispositivo MANTA contiene materiales biorreabsorbibles que no se pueden volver a utilizar ni volver a esterilizar. La reutilización o la reesterilización pueden causar degradación de la integridad del dispositivo, lo que puede provocar un fallo del dispositivo que puede provocar lesiones al paciente, enfermedades o la muerte. 8) No utilice el dispositivo MANTA donde se haya producido contaminación bacteriana de la vaina del procedimiento o de los tejidos circundantes, ya que esto puede provocar infección. 9) No utilizar si el sistema de entrega MANTA se tuerce. 11) No infle un balón contralateral en la arteria femoral o ilíaca durante el intercambio de Vainas MANTA o el procedimiento de Cierre MANTA. 12) No use MANTA si ha habido una punción de la arteria femoral en el mismo vaso en los 30 días anteriores, una reciente punción de la arteria femoral en la misma ingle que no ha sanado adecuadamente y/o una colocación reciente (<30 días) del dispositivo de cierre vascular en la misma arteria femoral. 13) No utilizar si el sitio de punción está en o distal a la bifurcación de la arteria femoral superficial y la arteria femoral profunda, ya que esto puede dar como resultado la (a) fijación de anclaje sobre la bifurcación o la colocación incorrecta, y/o (b) deposición de colágeno en el vaso. 14) No utilizar si hay una dilatación difícil desde el acceso inicial a la arteria femoral (por ejemplo, dilatadores dañinos o plegados) mientras se dilata el paso hasta el dispositivo de diámetro grande. La dilatación difícil del tracto de punción debido al tejido cicatricial puede provocar hinchazón del tejido circundante, lo que compromete la precisión de la profundidad de punción determinada durante el procedimiento de ubicación de la punción. 15) No utilizar si la inserción de vaina se encuentra en un vaso que no sea la arteria femoral. 16) No utilizar si hay marcada tortuosidad de la arteria femoral o ilíaca. 17) No utilizar si el paciente tiene obesidad marcada o caquexia (IMC>40 kg/m2 o <20 kg/m2). 18) No use si el paciente tiene presión arterial postprocedimiento>180 mmHg que no se puede bajar antes de cerrar el sitio de acceso. 19) No utilizar en pacientes que no puedan ser adecuadamente anticoagulados para el procedimiento. 20) No utilice el dispositivo MANTA en pacientes con alergias conocidas a productos de la especie bovina, productos de colágeno y/o colágeno, polímeros de ácido poliglicólico o poliláctico, acero inoxidable o níquel.
PRECAUCIONES: 1) El dispositivo MANTA sólo debe ser utilizado por un médico autorizado o un proveedor de atención médica capacitado en el uso de este dispositivo. 2) Este dispositivo contiene un pequeño bloqueo radiopaco de acero inoxidable que se implanta en el tracto de punción. Consulte la información de MRI en estas instrucciones de uso y la tarjeta de implante del paciente. 3) En caso de que el sangrado del sitio de acceso femoral persista después del uso del dispositivo MANTA, el médico debe evaluar la situación. Conforme a la evaluación médica de la cantidad de sangrado, use la compresión manual o mecánica, la aplicación de la presión del balón desde un sitio de acceso secundario, la colocación de un stent cubierto y/o la reparación quirúrgica para obtener la hemostasia.
POSIBLES EVENTOS ADVERSOS: Se han identificado los siguientes posibles eventos adversos relacionados con el despliegue de Dispositivos de Cierre Vascular: 1) Isquemia de la pierna o estenosis de la arteria femoral. 2) Trauma local a la pared de la arteria femoral o ilíaca, como la disección. 3) Sangrado retroperitoneal como resultado del acceso por encima del ligamento inguinal o el borde más inferior de la arteria epigástrica (IEA). 4) Perforación de arterias iliofemorales, causando sangrado/hemorragia. 5) Formación de trombosis o embolia. 6) Daño o neuropatía del nervio. 7) Otras complicaciones en el sitio de acceso que conducen a hemorragias, hematomas, seudoaneurismas o fístula arteriovenosa, que posiblemente requieran transfusión sanguínea, reparación quirúrgica y/o intervención endovascular. Los Posibles Eventos Adversos asociados con cualquier intervención de diámetro interno grande, incluido el uso del Dispositivo de Cierre Vascular MANTA, incluyen, entre otros: Daño arterial; Fístula arteriovenosa; Bradicardia; Síndrome del compartimento; Muerte relacionada con el procedimiento; Trombosis de la vena profunda; Equimosis; Edema; Infección en el sitio de punción que puede requerir antibióticos u hospitalización prolongada; Respuesta inflamatoria; Sangrado arterial tardío; Exudación del sitio de punción; Presión en la región de la ingle/sitio de acceso; laceración del vaso o trauma; Dehiscencia de la herida.
Consulte las instrucciones de uso para obtener información completa sobre el producto.
PRECAUCIÓN: Las leyes federales (de los Estados Unidos) restringen la venta de este dispositivo solo por parte de médicos o por orden de ellos.
No todos los productos están disponibles en todas las regiones. Comuníquese con el Servicio de atención al cliente para conocer la disponibilidad en su región.
Teleflex, the Teleflex logo, and MANTA are trademarks or registered trademarks of Teleflex, el logotipo de Teleflex y MANTA son marcas comerciales o marcas registradas de Teleflex Incorporated o sus afiliadas en los EE. UU. o en otros países. Las demás marcas comerciales o marcas registradas son propiedad de sus respectivos dueños.
MC-005922 LA EN Rev 0 Revisado: 09/2019.